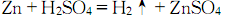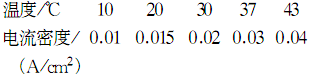化學(xué)性質(zhì)
中文名 鋅
外文名 zinc
分子量 65.38
CAS登錄號 7440-66-6
物性數(shù)據(jù)
1.性狀:淺灰色的細(xì)小粉末
2.熔點(diǎn)(℃):419.6
3.沸點(diǎn)(℃):907
4.相對密度(水=1):7.13
5.飽和蒸氣壓(kPa):0.13(487℃)
6.臨界壓力(MPa):290.4
7.辛醇/水分配系數(shù):-0.47
8.引燃溫度(℃):500
9.爆炸上限(%):暫無資料
10.爆炸下限(%):212~284mg/m3
11.溶解性:不溶于水,溶于酸�����、堿�����。
毒理學(xué)數(shù)據(jù)
1.急性毒性 暫無資料
2.刺激性 暫無資料
3.其他 TDLo:25mg/kg(大鼠氣管內(nèi))
生態(tài)學(xué)數(shù)據(jù)
1.生態(tài)毒性 暫無資料
2.生物降解性 暫無資料
3.非生物降解性 暫無資料
分子結(jié)構(gòu)數(shù)據(jù)
暫無
計(jì)算化學(xué)數(shù)據(jù)
1.疏水參數(shù)計(jì)算參考值(XlogP):無
2.氫鍵供體數(shù)量:0
3.氫鍵受體數(shù)量:0
4.可旋轉(zhuǎn)化學(xué)鍵數(shù)量:0
5.互變異構(gòu)體數(shù)量:無
6.拓?fù)浞肿訕O性表面積0
7.重原子數(shù)量:1
8.表面電荷:0
9.復(fù)雜度:0
10.同位素原子數(shù)量:0
11.確定原子立構(gòu)中心數(shù)量:0
12.不確定原子立構(gòu)中心數(shù)量:0
13.確定化學(xué)鍵立構(gòu)中心數(shù)量:0
14.不確定化學(xué)鍵立構(gòu)中心數(shù)量:0
15.共價(jià)鍵單元數(shù)量:1
性質(zhì)與穩(wěn)定性
1.原子半徑125皮米�����,第一電離能915kJ/mol����,電負(fù)性1.6���。硬度2.5�����,有延展性�����,良好的傳熱��、導(dǎo)電性�����,鋅燃燒時(shí)有藍(lán)綠色火焰��。高溫時(shí)跟水蒸汽反應(yīng)放出氫氣�。加熱時(shí)可跟鹵素����,硫等反應(yīng)���。易與酸反應(yīng),但高純鋅反應(yīng)慢�,若加入少量硫酸銅溶液,或跟銅、鎳���、鉑等金屬接觸時(shí),反應(yīng)加快�����。溶于強(qiáng)堿溶液�,化學(xué)性質(zhì)比較活潑。
2.室溫時(shí)在空氣中較穩(wěn)定�����。在潮濕空氣中生成一層灰色堿式碳酸鋅�,可作保護(hù)膜。
3.穩(wěn)定性 穩(wěn)定
4.禁配物 胺類����、硫����、氯代烴、強(qiáng)酸�、強(qiáng)堿���、氧化物、強(qiáng)氧化劑�、水、堿金屬氫氧化物
5.避免接觸的條件 潮濕空氣
6.聚合危害 不聚合
貯存方法
儲存注意事項(xiàng) 儲存于陰涼�、干燥���、通風(fēng)良好的專用庫房內(nèi)��,遠(yuǎn)離火種����、熱源�。庫溫不超過32℃,相對濕度不超過75%�����。包裝密封���。應(yīng)與氧化劑�、酸類�、堿類��、胺類���、氯代烴等分開存放,切忌混儲����。采用防爆型照明、通風(fēng)設(shè)施�����。禁止使用易產(chǎn)生火花的機(jī)械設(shè)備和工具���。儲區(qū)應(yīng)備有合適的材料收容泄漏物�。
安全信息
產(chǎn)品危害
侵入途徑:吸入��、食入�����。
吸入會引起口渴���、干咳�、頭痛�、頭暈、高熱�����、寒戰(zhàn)等��。粉塵對眼有刺激性�?���?诜碳の改c道。長期反復(fù)接觸對皮膚有刺激性�。
安全措施
1.貯于陰涼干燥處,遠(yuǎn)離火種����、熱源�。
2.與氧化劑、胺類�、硫��、磷、酸堿類分儲���。
3.滅火:干粉���、干砂。禁用水和泡沫��。
合成方法
1.真空下降360g金屬鋅緩慢加入到3340ml15%的硫酸溶液中�,加熱到70℃進(jìn)行反應(yīng)。
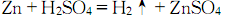
當(dāng)H2不再溢出后�,用1200ml水稀釋,制的硫酸鋅溶液����,取出50ml,其余備用��。在50ml稀釋溶液中加入4g碳酸鈉�����,析出的碳酸鋅沉淀用水洗滌三次(每次300ml)�,備用���。取7.5g七水合硫酸亞鐵溶于500ml水中,并用1ml優(yōu)級純硫酸酸化����,加熱����,逐滴加入30%的過氧化氫使溶液中Fe2+離子全部轉(zhuǎn)為Fe3+離子。將制的的硫酸鐵溶液加到上述備用的硫酸鋅溶液中����,并在攪拌下加入制好的碳酸鋅沉淀,然后在快速攪拌下加熱至30-40oC���,靜置��,待溶液澄清后,過濾【除去吸附有As��、P���、Sb等雜質(zhì)的Fe(OH)3沉淀】�����。濾液進(jìn)行電解并調(diào)節(jié)PH值���,使剛果紅稍稍變藍(lán)���。電解時(shí)以優(yōu)級純或鋅片作為陰極���,工業(yè)鋅作為陽極,兩極間距2-3cm���,兩極間電壓6V��,電流密度取決于電解液溫度�����。
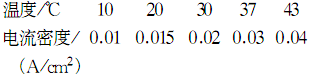
在析出200g鋅后�,電解液必須再按上述方法重新用硫酸鐵和碳酸鋅進(jìn)行處理�����。
2.制備鋅是以閃鋅礦ZnS為主要原料,通過冶煉而制得����。工業(yè)上通常是將ZnS氧化焙燒成具有良好反應(yīng)活性的氧化物。然后采用熱還原法和電解法來制得鋅����。將由鋅焙燒塊和煤粉制成的爐料,投入至1300~1350℃的煉鋅爐內(nèi)進(jìn)行反應(yīng)�����,還原反應(yīng)所生成的金屬鋅蒸氣����,經(jīng)導(dǎo)管通入鋅冷凝器,捕集得金屬鋅���。此法所得到的金屬鋅雜質(zhì)含量較高����,要獲得較純的鋅����,還需進(jìn)行真空蒸餾�����。
3.將焙燒料中的氧化鋅用硫酸溶解���,通過氧化除鐵,鋅粉置換除鈷�、銅、鎳等雜質(zhì)后����,置于電解槽內(nèi)�����,以鉛作陽極����,鋁板作陰極。電解時(shí)����,金屬鋅沉積在鋁板上���,將其剝離下來便成為產(chǎn)品。用電解法生產(chǎn)的金屬鋅純度可達(dá)99.99%�����。
上下游產(chǎn)品信息
表征圖譜
相關(guān)文獻(xiàn)
用途
1.用作分析試劑�,如作還原劑,用于砷���、銅����、硝酸鹽等測定����。
2.與乙酸、鹽酸�、硫酸、堿���、水(含氯化按)等共用作還原劑�。鋅粉蒸餾����。制有機(jī)鋅化合物���。Reformatsky反應(yīng)。由苯甲醛制苯基卡賓等�����。
3.用作催化劑�����、還原劑�����,用于有機(jī)合成�����,也用于電鍍鋅和制備有色金屬合金��。