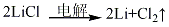化學(xué)性質(zhì)
1.性狀:銀白色軟金屬����。
2.熔點(diǎn)(℃):180.54
3.沸點(diǎn)(℃):1317~1342
4.相對密度(水=1):0.534(20℃)
5.飽和蒸氣壓(kPa):0.13(723℃)
6.臨界壓力(MPa):68.9[6]
7.溶解性:不溶于烴類,溶于硝酸���、液氨���。
毒理學(xué)數(shù)據(jù)
1.急性毒性[8] LD50:1000mg/kg(小鼠腹腔)
2.刺激性 暫無資料
3.致突變性[9] 細(xì)胞遺傳學(xué)分析:人714mg/kg(8周,間斷)
生態(tài)學(xué)數(shù)據(jù)
1.對水有稍微危害,不要讓未稀釋的或者大量的產(chǎn)品接觸地下水�、水道或者污水系統(tǒng)。
2.生態(tài)毒性 暫無資料
3.生物降解性 暫無資料
4.非生物降解性 暫無資料
分子結(jié)構(gòu)數(shù)據(jù)
1��、摩爾折射率:無可用的
2�、摩爾體積(cm3/mol):無可用的
3、等張比容(90.2K):無可用的
4���、表面張力(dyne/cm):無可用的
5、介電常數(shù):無可用的
6���、極化率(10-24cm3):無可用的
7�、單一同位素質(zhì)量:7.016004 Da
8���、標(biāo)稱質(zhì)量:7 Da
9��、平均質(zhì)量:6.941 Da
具有強(qiáng)還原性�,空氣中極易氮化�,遇水劇烈燃燒或爆炸。避免與鹵素�、酸類、氧����、氯代烴�、硫��、磷接觸���。室溫時(shí)在干燥的空氣中幾乎不能被氧化����。對水的反應(yīng)也很慢�,在堿金屬中反應(yīng)性最低。但是����,與其他堿金屬不同的是由于能與氮反應(yīng),所以氣體介質(zhì)應(yīng)該使用氬或氦�。室溫時(shí)在干燥空氣中不易被氧化,浮在水上而不下沉�,與水反應(yīng)緩慢,與氮?dú)夥磻?yīng)形成氮化鋰��。干燥的石墨粉可作鋰滅火劑���。
安全信息
危險(xiǎn)運(yùn)輸編碼:暫無
危險(xiǎn)品標(biāo)志:暫無
安全標(biāo)識(shí):暫無
危險(xiǎn)標(biāo)識(shí):暫無
合成方法
1.電解法:以無水氯化鋰為原料�,加入電解槽中加熱熔融進(jìn)行電解,制得金屬鋰成品�。其
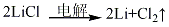
2.采用真空蒸餾法。以金屬鋰為原料���,在低溫下長時(shí)間蒸餾���,在冷卻管上析出含雜質(zhì)較多的鋰。接著�����,將裝置冷卻并充滿精制的氬氣���,換上新的冷卻管,抽成真空(絕壓≤0.1kPa)����,用比以前更高的溫度進(jìn)行蒸餾。最后將裝置充分冷卻后����,充滿氬氣,用刮刀等把從冷卻管上提純的金屬鋰刮下來��,將這種蒸餾操作反復(fù)進(jìn)行,制得高純鋰成品���。
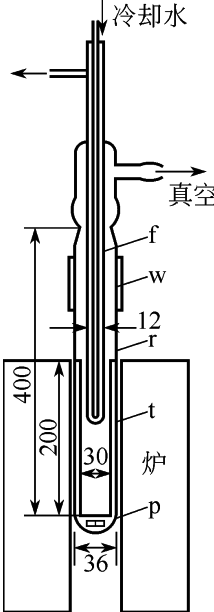
鋰提純方法:用真空蒸餾法提純金屬鋰�。提純裝置如圖Ⅰ-1所示��。在石英管r中放入低碳鋼制備的坩堝�����,中間以小瓷片p墊起�,將石英管與坩堝隔開。坩堝中插入鋼鎳或銅制的冷卻管f�,冷卻管外面有一層玻璃管,連帶磨口蓋��,將石英管密封��,并與真空泵相連�,磨口部分以蛇形管w冷卻。向坩堝中加入待提純的金屬鋰�,為了避免氧化物、氮化物對產(chǎn)品的污染���,可在金屬鋰上鋪一薄層已經(jīng)過脫脂的鋼纖維����。維持低溫長時(shí)間蒸餾,在冷卻管f上即有鋰析出�����。但所得的鋰中揮發(fā)性雜質(zhì)較多��。待裝置冷卻后通入高純氬氣���,打開磨口蓋�,取出冷卻管�����,連同磨口蓋外套玻璃一并換上一付新的冷卻管��,升高溫度進(jìn)行減壓蒸餾(真空度≤0.133Pa)���。為了保證鋰的純度,坩堝中的鋰不能全部蒸干凈�����,才能達(dá)到分離不易揮發(fā)性雜質(zhì)的目的。待裝置冷卻后�����,在氬氣氛圍中打開磨口蓋�����,在通有氬氣的干燥箱中���,用刮刀將冷卻管上的純凈金屬鋰刮下�����。將上述操作反復(fù)進(jìn)行即可得到高純度的金屬鋰�����。
以下是圖1-1鋰的蒸餾裝置(圖中單位為毫米)
上下游產(chǎn)品信息
表征圖譜
相關(guān)文獻(xiàn)
用途
1.用于生產(chǎn)各種鋰電池�����、輕質(zhì)鋰鋁合金���、冶金的脫氣劑��,合成橡膠�����、制藥工業(yè)��、化工�����、醫(yī)藥等�����。
2.在化工�����、醫(yī)藥��、有色合金、合成橡膠工業(yè)中用作催化劑����。是生產(chǎn)高純鋰的原料�。
3.用作鋰電池����、還原劑與氫化劑、合金硬化劑��、銅和銅合金中脫氧劑��,也用于有機(jī)合成